
Sovint, al percebre els tumors com una lesió, el teixit connectiu que envolta el tumor es reestructura com en el procés de reparació de ferides. Aquesta reacció és induïda per molècules (com la citocina TGFβ) alliberades per cèl·lules epitelials tumorals o de ferides que actuen sobre fibroblastes estromals i és característica de tumors epitelials en òrgans tous, com la mama, el pulmó o l'intestí. Com a resultat d'aquesta reacció, es genera un estroma peritumoral desmoplàsic ric en fibres de fibronectina i col·lagen. La desmoplasia associada a tumors persisteix si el tumor no remet, cosa que facilita la mobilitat de les cèl·lules tumorals, la invasió dels teixits adjacents i, en última instància, la intravasació als vasos sanguinis o limfàtics. Per tant, la desmoplàsia tumoral s'associa amb la formació de metàstasi. La nostra recerca té com a objectiu entendre aquesta resposta i la influència de les noves propietats químiques i físiques de l'entorn tumoral en la formació de metàstasi.
Els nostres resultats ens han permès descriure com els fibroblasts associats a tumors (CAF) incrementen la composició, rigidesa i organització tridimensional de les fibres extracel·lulars i com aquests paràmetres promouen la invasió tumoral. A nivell molecular, hem descrit que l'activitat d'un factor de transcripció anomenat Snail1 regula de manera anàloga la desmoplàsia causada pels CAF, els fibroblasts associats a ferides i els fibroblasts activats en els processos fibròtics. Snail1 és un repressor transcripcional però en aquests fibroblasts també pot actuar com a activador transcripcional i com a factor d'splicing. Hem definit alguns elements moleculars, com la subunitat ReIA (p65) del factor nuclear-kB (NF-kB), PARP1 i PRMTs1-4, que col·laboren amb Snail1 per incrementar la transcripció de molècules de la matriu extracel·lular, com la fibronectina. Snail1 també és necessari per a l'activitat enzimàtica de RhoA, que controla la reorganització del citoesquelet dels fibroblasts i permet la polimerització de les fibres extracel·lulars, tot i que el mecanisme encara ha d'estudiar-se en detall.
Analitzant carcinomes infiltrants de mama hem demostrat la rellevància de Snail1 en la progressió del tumor. La detecció immunohistoquímica de Snail1 en els fibroblasts de l'estroma tumoral és un indicador molt fidel de mal pronòstic. Per interès terapèutic, hem aprofitat les dades que indiquen que les metiltransferases PRMT1 i 4 col·laboren amb Snail1 per reduir la formació de metàstasi mitjançant la injecció d'inhibidors de la metiltransferasa en un model de càncer de ratolí (figura 1).
Amb la nostra investigació actual busquem millorar el coneixement de la regulació molecular dels fibroblasts associats a tumors. Estem explorant les accions de Snail1 en la matriu extracel·lular controlant l'splicing alternatiu de les molècules estructurals. Per tant, estem descrivint com l'splicing està regulat per Snail1 i quins papers desenvolupen algunes variants d'splicing en les propietats metastàtiques de les matrius.
Sospesem la possibilitat d'utilitzar inhibidors específics d'splicing basats en nucleòtids modificats com a eines farmacològiques antimetastàtiques, ja que és una estratègia que s'utilitza amb èxit en patologies associades a variants d'splicing anormals.
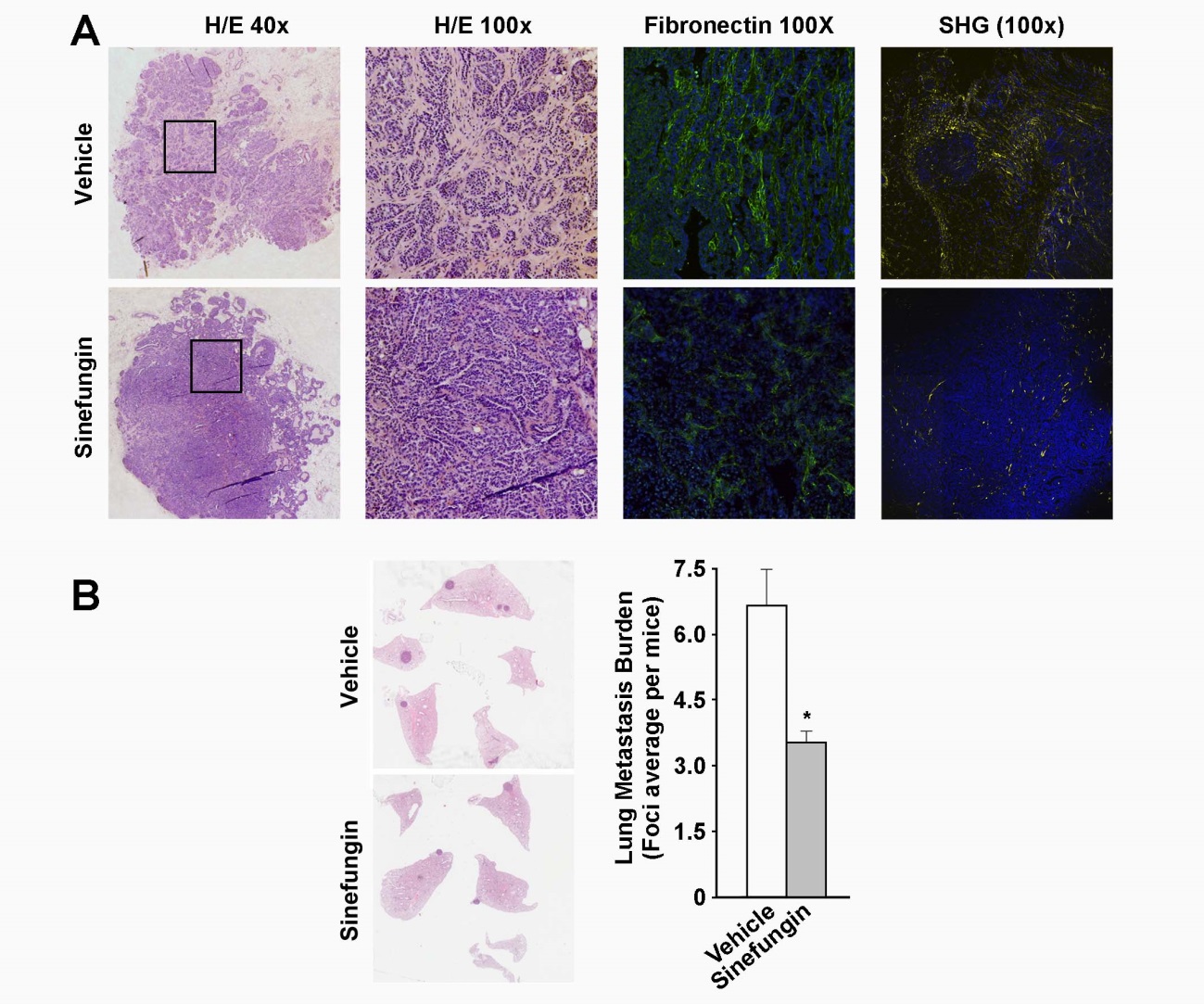
Figura 1. La sinefungina prevé la reacció estromal i disminueix la metàstasi en ratolins. A) Tumors primaris de mama en ratolins tractats o no amb sinefungina van ser analitzats per immunohistoquímica (tinció d'hematoxilina-eosina), immunofluorescència (fibronectina) o generació de segon harmònic (col·lagen). El component estromal dels tumors es va reduir en els ratolins tractats. B) Es van explicar els focus metastàtics pulmonars. El gràfic mostra que el tractament amb sinefungina redueix la càrrega metastàtica en els pulmons. De Sala et al., 2019.
Quatre publicacions recents del grup són:
© Institut Hospital del Mar
d'Investigacions MèdiquesAvís Legal i Política de Privacitat | Política de cookies | Mapa web | Accessibilitat | Adreça / Accessos | Contacte